A Fogalomtár jelenleg revízión esik át, az egyes szócikkek tartalmának javítása folyamatban van.

A - B - C - D - E - F - G - H - I - K - M - N - O - P - Q - R - S - Sz - T - V
Szójegyzék:
abszolút kockázat - abszolút kockázat-csökkentés és -növelés - AGREE kérdőív >>> beavatkozás hatásossága - bizonyíték-piramis - bizonyítékokon alapuló orvoslás >>> CASP-kérdőív - CINAHL adatbázis - CONSORT közlemény >>> DELBI-kérdőív - dichotóm változó / bináris változó - diszkrét változó >>> elfogultság kockázata - erdő-grafikon - esélyérték - esélyhányados - eset-kontroll vizsgálat - esetsorozat >>> folytonos változó >>> GRADE >>> hatásmutató / kimenetel - hatásnagyság és hatástalanság - heterogenitás és homogenitás - hipotézisvizsgálat >>> IMRAD felépítés - irányelv >>> keresztmetszeti vizsgálat - kezelendő betegek száma - kezelési-szándék elemzés - khí négyzet-próba - kockázati tényező / rizikófaktor - kohorsz vizsgálat - kontingenciatáblázat - konfidencia-szint - korreláció >>> meta-analízis - meta-regresszió >>> nullhipotézis - normális eloszlás >>> orvosi tárgyszavak >>> p-érték - PICO-modell - placebo - PRISMA módszertani ajánlás - protokoll-szerinti elemzés - PubMed adatbázis >>> QUOROM közlemény >>> randomizált, kontrollált vizsgálat - regresszió-analízis - relatív gyakoriság - relatív kockázat - relatív kockázat-csökkentés és -növelés >>> Scopus adatbázis >>> szignifikancia-szint - szisztematikus áttekintés >>> t-eloszlás - t-próba >>> valószínűség - véletlenszerű besorolás / randomizálás
A
abszolút kockázat
(Absolute Risk, AR)
Az abszolút kockázat egy esemény adott körülmények között történő bekövetkezésének valószínűsége. Példa: ha a rosszindulatú daganatos megbetegedések 10.000 fő között 600 fő esetén alakulnak ki, akkor ezek abszolút kockázata (600/10.000) = 0,06. Az abszolút kockázat tehát 6%.
abszolút kockázat-csökkentés és -növelés
(Absolute Risk Reduction, ARR / Absolute Risk Increase, ARI)
Az abszolút kockázat-csökkentés egy kezelés hatékonyságának mutatója, az egyik leghasznosabb módja a kutatási eredmények bemutatásának, és a döntéshozatal segítésének. Egy személy csökkentheti saját abszolút kockázatát, ha megfelelő lépéseket tesz, például kevesebb alkoholt fogyaszt (májbetegségek) vagy egészségesebben étkezik (szív- és érrendszeri problémák, cukorbetegség). Tekintsük az alábbi kontingenciatáblázatot:
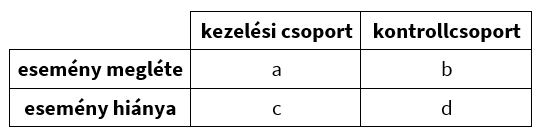
Ha egy kezelés (intervenció) csökkenti egy káros egészségügyi kimenetel kockázatát (pozitív hatás), akkor az abszolút kockázat-csökkentés (ARR) a táblázat jelölései alapján:
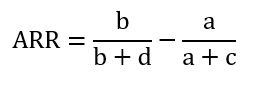
Példa: Ha egy 10.000 fős kezelési csoportban egy betegség 560 főnél, illetve egy ugyanekkora kontrollcsoportban 660 főnél jelentkezik, akkor az abszolút kockázat-csökkentés: (660/10.000) - (560/10.000) = 0,066-0,056 = 0,01. A kezelés tehát 1%-kal csökkentette a betegség abszolút kockázatát.
Ha egy kezelés növeli egy káros egészségügyi kimenetel kockázatát (negatív hatás), akkor az abszolút kockázat-növelés (ARI) a táblázat jelölései alapján:

AGREE kérdőív
(Appraisal of Guidelines Research and Evaluation)
Az irányelvek kutatásának és értékelésének megítélése. Az AGREE a gyakorlati irányelvek kidolgozásának folyamatát és a beszámolókészítés minőségét értékeli. Célja, hogy keretet adjon a gyakorlatban használt klinikai iránymutatások minőségének értékeléséhez. Az AGREE eszközt a következő csoportok számára tervezték:
- Politikai döntéshozóknak, hogy segítsen eldönteni mely iránymutatások ajánlhatók a gyakorlatban való alkalmazásra.
- Irányelv-fejlesztőknek egy rendszerezett és szigorú fejlesztési módszertan követéséhez, valamint önértékelési eszközként irányelveik megalapozottságának biztosításához.
- Egészségügyi szolgáltatóknak, akik az ajánlások elfogadása előtt felmérést kívánnak végezni.
- Oktatóknak vagy tanároknak, hogy elősegítsék az egészségügyi szakemberek kritikai értékelő készségének fejlesztését.
B
beavatkozás hatásossága
(intervention effectiveness)
Egy kezelés, például egy új gyógyszer alkalmazása során megfigyelt változás egy klinikai vizsgálatban mért egészségügyi mutatóban egy kontrollhoz képest. Fontos megkülönböztetni a hatásfok (efficacy) és a hatékonyság (effectiveness) fogalmakat. A hatásfok a kezelés elméleti (legjobb körülmények között meghatározott) hatása, a hatékonyság pedig a gyakorlati (való életben mérhető) hatás, mely figyelembe veszi a kezelés költségeit, megvalósíthatóságát stb. is.
bizonyíték-piramis
(evidence pyramid)
Az információkeresés ún. 4S piramison alapuló stratégiája. A piramis csúcsán helyezkednek el a döntéshozást segítő számítógépes rendszerek (systems), alattuk a bizonyítékokon alapuló folyóirat-absztraktok (synopses), ezek alatt pedig a Cochrane áttekintések (sytheses). Legalul találhatók a folyóiratokban közzétett egyedi tanulmányok (studies).
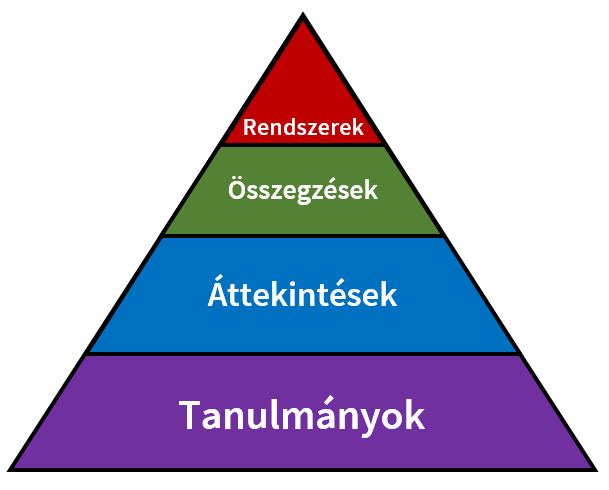
bizonyítékokon alapuló orvoslás
(Evidence-Based Medicine, EBM)
A bizonyítékokon alapuló orvoslás (EBM) az egyes betegek ellátásával kapcsolatos döntések meghozását a jelenleg elérhető legjobb minőségű klinikai eredményekre kívánja alapozni. Az EBM több tudományágat ötvöző (interdiszciplináris) módszer, mely randomizált, kontrollált vizsgálatok, meta-analízisek, szisztematikus áttekintések, kockázat-haszon elemzések és döntéselemzések segítségével értékeli az orvosi szakirodalomból származó bizonyítékokat. Célja olyan bizonyítékokon alapuló, határozott, gyakorlati irányelvek megtervezése, melyek a betegek érdekeit tartják szem előtt. A bizonyítékok értékelése és rangsorolása a GRADE módszerrel történik.
C
CASP-kérdőív
(Critical Appraisals Skills Programme)
A CASP egy ellenőrzőlista, mely a közétett tanulmányok megbízhatóságának, relevanciájának és eredményeinek felmérésében nyújt segítséget. Általános eszköz a kutatási módszerek erősségeinek és korlátainak értékelésére: alkalmazható szisztematikus áttekintések, kohorsz vizsgálatok, eset-kontroll vizsgálatok és randomizált, kontrollált vizsgálatok esetén is.
CINAHL adatbázis
(Cumulative Index to Nursing and Allied Health Literature)
A CINAHL az ápolási szakirodalmat jegyzékét tartalmazó, szabadon elérhető adatbázis. Hozzáférést biztosít több mint 3.900 folyóirathoz, és 1.000.000 közleményhez, többek között az ápolás, az alternatív terápiák, a biomedicina és az egészségügyi igazgatás témakörében.
CONSORT közlemény
(Consolidated Standards of Reporting Trials)
A CONSORT magában foglalja a CONSORT Csoport által, a szerzők számára megfogalmazott alapvető elvárásokat, amelyek a randomizált, kontrollált vizsgálatok (RCT-k) nem megfelelő jelentése során fellépő problémákat hivatott mérsékelni. A CONSORT 2010 közleménye egy 25 elemből álló ellenőrző listát és egy folyamatábrát tartalmaz. Az ellenőrző lista a vizsgálat tervezettségét, az adatok elemzését és az eredmények értelmezését, a folyamatábra pedig a vizsgálatba bevont összes résztvevő nyomon követésének elvárt módszerét jeleníti meg.
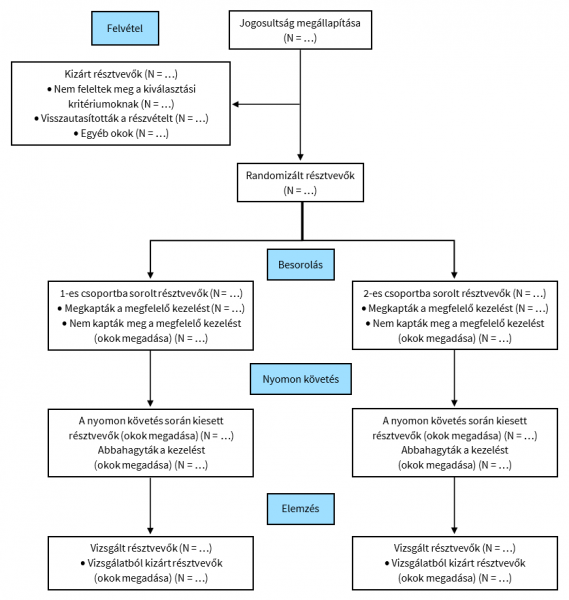
D
DELBI-kérdőív
(Deutsche Instrument zur methodischen Leitlinien-Bewertung)
Német kutatók által létrehozott eszköz az irányelvek módszertani értékelésére. A 2003 és 2005 között kifejlesztett DELBI ellenőrző lista a klinikai gyakorlatban használt irányelvek minőségének értékelésére szolgál. Az alapvető minőségi elvárások megegyeznek az AGREE eszköz feltételeivel. A kérdések 8 csoportba lettek sorolva, ezek az alábbiak:
- Hatályosság és cél
- Az érintett felek bevonása
- A fejlesztések módszertani szigorúsága
- Átláthatóság és bemutatás
- Általános alkalmazhatóság
- Szerkesztői függetlenség
- Alkalmazhatóság a német egészségügyi rendszerben
- A fejlesztések módszertani szigorúsága meglévő irányelvek használatakor
dichotóm változó / bináris változó
(dichotomous variable / binary variable)
Matematikai vagy statisztikai változó, mely csak két értéket vehet fel. A legegyszerűbb példa dichotóm változóra a biológiai nem (nő, férfi), valamilyen tuladjonság megléte (igen, nem), vagy egy vizsga eredménye (megfelelt, nem felelt meg).
diszkrét változó
(discrete variable)
Matematikai vagy statisztikai változó, mely csak adott helyeken vehet fel értéket, például egész számokat, de a kategorikus változók is ide tartoznak. Diszkrét változó az életkor (a betöltött életévek száma egész szám), a született gyermekek száma vagy a családi állapot (nőtlen, hajadon, házas, elvált stb.).
E
elfogultság kockázata
(Risk of Bias, RoB)
Egy szisztematikus áttekintés vagy meta-analízis egyes bevont tanulmányainak kritikus minőség-értékelésére használt eszköz. A kockázat 3 szintjét ("magas", "alacsony", "tisztázatlan"), valamint a torzítás 6 fő kategóriáját különbözteti meg:
- Kiválasztási torzítás (selection bias) - A résztvevők csoportba sorolása nem teljesen véletlenszerű módon történt, illetve nem sikerült megvalósítani a besorolás titkosságát.
- Teljesítménybeli torzítás (performance bias) - A résztvevők és az alkalmazottak ismerik a vizsgálati elrendezést, vagyis az ún. vakosítás (blinding) nem történt meg.
- Érzékelési torzítás (detection bias) - A vizsgálati eredmények kiértékelését végző kutatók ismerik, hogy az adatok mely kezelési csoportokhoz tartoznak.
- Lemorzsolódási torzítás (attrition bias) - A vizsgálatból kieső résztvevők miatt hiányossá válnak a kutatási eredmények.
- Közlési torzítás (reporting bias) - Bizonyos kiválasztott (például statisztikailag nem szignifikáns) kutatási eredmények közlésének elmulasztása.
- Egyéb torzítás - A fenti kategóriáktól eltérő források.
erdő-grafikon
(forest-plot)
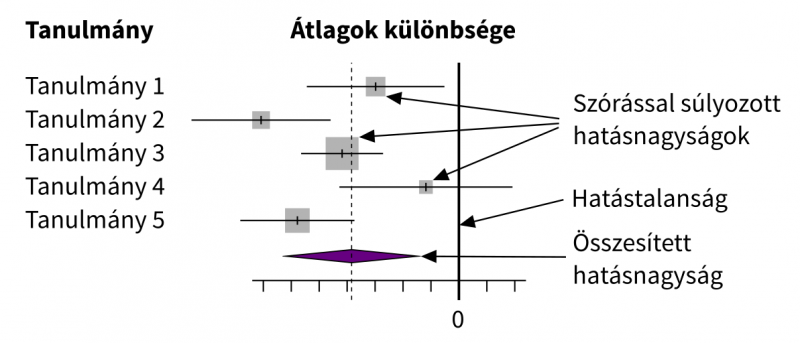
Az erdő-grafikonok a meta-analízisek eredményeinek megjelenítésére szolgáló ábrák. Az összefoglalt tanulmányok hatásnagyságait a vizsgálati adatok szórásával súlyozzák, ezekből áll elő az összesített hatásnagyság. Ha egy vizsgálatban nem tapasztalható különbség a kezelési és a kontroll-csoport között, akkor ennek hatásnagysága a hatástalanságot jelentő 0 értékre esik. Megjegyzés: a Cochrane Együttműködés logója is egy erdő-grafikont ábrázol.
esélyérték
(odds)
Egy esemény bekövetkezésének valószínűségét fejezi ki, kiszámításához el kell osztani azon esetek számát, amikor az esemény bekövetkezik azon esetek számával, amikor az esemény nem következik be - ellentétben a relatív valószínűséggel, ahol az osztó az összes eset. Olykor két, kettősponttal elválasztott számmal szokták leírni. Példa: a hatos dobásának esélyértéke egy szabályos dobókockával 1:5, vagyis ötször nagyobb valószínűséggel lesz a dobott érték hatostól eltérő, mint hogy hatos lesz.
esélyhányados
(Odds Ratio, OR)
Az esélyhányados két tulajdonság (például egy betegség megléte és egy rizikófaktor) összefüggését határozza meg, az esélyértékek hányadosa. A relatív kockázat (RR) az esélyhányados (OR) segítségével becsülhetővé válik eset-kontroll vizsgálatokban. Tekintsük az alábbi kontingenciatáblázatot:
 Az esélyhányados (OR) a táblázat jelölései alapján:
Az esélyhányados (OR) a táblázat jelölései alapján:
![]()
Értéke az alábbi három tartomány egyikébe esik:
- OR < 1: a két tulajdonság negatívan korrelál, vagyis az egyik tulajdonság megléte csökkenti, hiánya pedig növeli a másik tulajdonság kockázatát.
- OR = 1: a két tulajdonság között nincs összefüggés.
- OR > 1: a két tulajdonság pozitívan korrelál, vagyis az egyik tulajdonság megléte növeli, hiánya pedig csökkenti a másik tulajdonság kockázatát.
Fontos megjegyezni, hogy az összefüggés nem jelent egyben ok-okozati kapcsolatot is.
Példa: a dohányzás köztudottan növeli a tüdőrák kockázatát. Tegyük fel, hogy a tüdőrák egy dohányzó csoporton belül 350 főnél alakul ki, 140 főnél pedig nem, illetve egy nemdohányzó csoporton belül 290 főnél alakul ki, 510 főnél pedig nem. Az esélyhányados ekkor: (350/290) / (140/510) = 1,21/0,27 = 4,481. A tüdőrák kialakulásának kockázata tehát több mint 4-szer akkora dohányzás esetén, mint anélkül.
eset-kontroll vizsgálat
(case–control study)
Az eset-kontroll vizsgálatok egy betegségben szenvedő csoportot (esetcsoport) és egy, az adott betegségben nem szenvedő csoportot (kontrollcsoport) hasonlítanak össze a betegséget kiváltó tényezők és rizikófaktorok szempontjából. A kórtörténetek visszakövetése miatt ún. retrospektív vizsgálatoknak is nevezik ezeket. Előnyük, hogy rövid idő alatt és olcsón elvégezhetők, hátrányuk pedig, hogy a kontrollcsoport megválasztása nagyon nehéz feladat, hiszen ekkor az a cél, hogy a kontrollcsoport csak az adott betegség megléte tekintetében különbözzön a beteg-csoporttól.
esetsorozat
(case series)
Az esetsorozatok hasonló kezelésben részesülő személyek esetjelentéséből állnak, melyek külön-külön az adott alany diagnózisáról, kezeléséről, és követéséről adnak részletes beszámolót. Leíró jellegű tanulmányok, melyek nem tartalmaznak analitikus elemzést (például hipotézisvizsgálatot), ezért eredményeik sem tekinthetők elfogultságtól menteseknek.
F
folytonos változó
(continuous variable)
Matematikai vagy statisztikai változó, mely egy adott értékétől végtelenül (infinitezimálisan) kis távolságra is felvehet értéket. A legkézenfekvőbb példa folytonos változóra a testmagasság, mely pontosságának csak a mérőeszköz pontossága szab határt (általában centiméter).
G
GRADE
(Grading of Recommendations Assessment, Development and Evaluation)
A GRADE egy átlátható keretrendszer a klinikai ajánlások és bizonyítékok összegzésének, kidolgozásának és kiértékelésének minősítésére. Négy szinjét különböztetjük meg a legmagasabb szintűnek tekintett „A” besorolástól a legalacsonyabb szintűnek tartott „D” besorolásig:
- "Magas": Magas minőségű, az elfogultság nagyon alacsony kockázatát mutató meta-analízisek, szisztematikus áttekintések és RCT-k eredményei, melyek közvetlenül alkalmazhatók a célpopulációra.
- "Közepes": Magas minőségű, az elfogultság nagyon alacsony kockázatát mutató eset-kontroll és kohorsz vizsgálatok eredményei, melyek közvetlenül alkalmazhatók a célpopulációra.
- "Alacsony": Az elfogultság magas kockázatát mutató meta-analízisek, szisztematikus áttekintések és RCT-k, vagy jól tervezett, az elfogultság alacsony kockázatát mutató eset-kontroll és kohorsz vizsgálatok eredményei, melyek közvetlenül alkalmazhatók a célpopulációra.
- "Nagyon alacsony": Az elfogultság magas kockázatát mutató eset-kontroll és kohorsz vizsgálatok eredményei, vagy esettanulmányok, szakértői vélemények.
H
hatásmutató / kimenetel
(outcome)
A hatásmutatók a klinikai vizsgálatok által mért biológiai mennyiségek, melyek lehetnek folytonos, diszkrét vagy kategorikus változók. A vizsgálatok fő célja az ún. elsődleges hatásmutatók mérése és kiértékelése, a kevésbé hangsúlyos változók a másodlagos hatásmutatók.
hatásnagyság és hatástalanság
(effect size)
A hatásnagyság az orvosi statisztikákban (meta-analízisekben) gyakran számolt mennyiség. Két csoportban (például kezelési és kontroll) az átlagos mért hatásmutatók közötti eltérés osztva a populációk összevont szórásával. Amennyiben nincs statisztikailag szignifikáns különbség a kezelési és a kontrollcsoport között, akkor a kezelés hatástalannak tekinthető.
homogenitás és heterogenitás
(heterogeneity and homogeneity)
Egy meta-analízisben vizsgált tanulmányok közötti eltérések mértéke. Ideális esetben az összes tanulmány egyforma tervezettségű lenne és hasonló módszereket alkalmazna, eredményeik pedig csak a kiküszöbölhetetlen mérési (szisztematikus) hibákban térnének el egymástól: ekkor homogének lennének. Az ezeken kívül fellépő hibák adják a tanulmányok mérhető heterogenitását.
hipotézisvizsgálat
(hypothesis test)
A hipotézisvizsgálat egy több lépésből álló statisztikai folyamat.
- Először határozzuk meg a megfelelő nullhipotézist (H0) és az ennek ellentmondó alternatív hipotézist (H1), majd vegyük figyelembe a vizsgált adatsor statisztikai feltételezéseit (az adatok függetlensége, normális eloszlása stb.).
- Válasszuk ki a megfelelő teszt-statisztikát (ez leggyakrabban a t-próba), mely a nullhipotézis és az alternatív hipotézis közötti választásban segít. Határozzuk meg a teszt-statisztika eloszlását, ami egyszerű esetben adott paraméterű t-eloszlást vagy normális eloszlást követ.
- Válasszuk meg a szignifikancia-szintet (α), ami a nullhipotézis hibás elvetésének (elsőfajú hiba) vagy hibás elfogadásának (másodfajú hiba) küszöbértéke (általában 5%). A szignifikancia-szint megfelel egy konfidencia-szintnek (γ = 1 - α) is (általában 95%). A teszt-statisztika eloszlásán belül két tartományt jelölhetünk ki: az egyik az ún. kritikus tartomány (valószínűsége α), amiben elvetjük a nullhipotézist, a másikban pedig nem.
- Számítsuk ki a teszt-statisztika alapján a megfigyelt értékekre vonatkozó t-értéket (tm). Amennyiben ez a tm-érték a kritikus tartományba esik, vessük el a nullhipotézist, ellenkező esetben tartsuk meg azt.
Egy másik megközelítés a p-érték használata. A nullhipotézist akkor vetjük el, ha a kiszámított p-érték kisebb, mint a szignifikancia-szint, ellenkező esetben megtartjuk azt.
I
IMRAD felépítés
(Introduction, Methods, Results And Discussion)
A tudományos publikációk legelterjedtebb általános dokumentum-szerkezete. Az egyes részek sorrendje és tartalma:
- Bevezetés (Introduction): a kutatás motivációja, célja, és a vizsgált hipotézis bemutatása
- Módszerek (Methods): a felhasznált anyagok és a résztvevők jellemzőinek leírása
- Eredmények (Results): a tanulmány kérdésének megválaszolása, a hipotézis megtartása vagy elvetése
- Diszkusszió (Discussion): az eredmények következményei, a jövőbeli kutatások lehetőségei
irányelv
(guideline)
Az irányelvek a protokollokhoz (előírásokhoz) és ajánlásokhoz hasonló eszközök, melyek alapvető fontosságúak a fejlesztési és alkalmazási stratégiák szempontjából. Szisztematikusan kifejlesztett állítások orvosok és betegek döntéshozatalának segítésére az adott körülmények között megfelelő egészségügyi ellátás biztosítása számára. Az irányelvekkel szemben támasztott követelmények kitérnek a gazdasági átláthatóságra, a költséghatékonyságra, a megalapozottságra, a következetességre, a megbízhatóságra, a rugalmasságra, az érthetőségre, a gyakorlati alkalmazhatóságra és a rendszeres frissítések biztosítására.
K
keresztmetszeti vizsgálat
(cross-sectional study)
A keresztmetszeti vizsgálatok egy adott időpontra vonatkozóan gyűjtenek adatokat. Előnyük, hogy gyors eredményeket szolgáltatnak és a teljes populációt vizsgálják, hátrányuk viszont, hogy időbeli korlátozottságuk miatt nem nyújtanak információt a betegségek okáról vagy lefolyásáról, sem a kezelések hatékonyságáról.
kezelendő betegek száma
(Number Needed to Treat, NNT)
A kezelendő betegek száma egy intervenció (általában egy gyógyszeres kezelés) hatékonyságának mérőszáma. Azok átlagos számát jelenti, akiket kezelni kell annak érdekében, hogy egy személy esetén egy további káros kimenetel (például stressz, daganat, stroke stb.) bekövetkezését megelőzzük, azaz megjelenlen a gyógyszer jótékony hatása. Minél kisebb ez a szám, annál hatékonyabb a kezelés. Tekintsük az alábbi kontingenciatáblázatot:

A kezelendő betegek száma (NNT) a táblázat jelölései alapján:
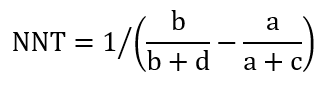
A kapott értéket felfelé kell kerekíteni, amennyiben az NNT nem egész szám. Példa: Tegyük fel, hogy egy 10.000 főből álló kontrollcsoportban 500 fő hal meg egy adott betegség következtében, egy ugyanekkora kezelési csoportban pedig 200 fő. A kezelendő betegek száma: 1/[(500/10.000)-(200/10.000)] = 1/(0,05-0,02) = 33,33 -> 34, vagyis átlagosan 34 ember kezelése esetén éli túl a betegséget egy olyan beteg, aki meghalt volna a betegség következtében. (Megjegyzés: a kezelendő szükséges betegek száma (NNT) az abszolút kockázat-csökkentés (ARR) reciproka.)
kezelési-szándék elemzés
(intention-to-treat analysis, ITT)
A kezelési csoportok összehasonlítása az összes résztvevővel, akik megkezdték a vizsgálatot. Minden véletlenszerűen besorolt résztvevőt figyelembe vesz, függetlenül attól, hogy mennyi ideig részesültek kezelésben, vagy kiléptek-e a vizsgálatból. A hiányzó adatokat általában az utoljára mért értékekkel pótolják.
khí négyzet-próba
(chi-squared test)
A khí négyzet-próba (χ2) egy statisztikai módszer, mely során hipotézisvizsgálatot hajtunk végre egy adatsoron. A nullhipotézis szerint a megfigyelt és a várt (valószínűségekkel megadható) értékek között nincs szignifikáns különbség.
kockázati tényező / rizikófaktor
(risk factor)
A kockázati tényező egy betegség kialakulásának valószínűségét növelő jellemző. Ilyen rizikófaktorok például szív- és érrendszeri megbetegedések esetén az egészségtelen étrend, a testmozgás hiánya stb., vagy daganatos megbetegedések esetén az örökölt (genetikai) hajlam, a dohányzás, életkor stb.
kohorsz vizsgálat
(cohort study)
Előre megtervezett, más néven prospektív vizsgálat, melyben a résztvevőket egy közös tulajdonság alapján csoportokba ún. kohorszokba sorolják. Például egy betegség kockázati tényezői alapján kohorszokba osztják a résztvevőket, majd hosszabb időn keresztül követik őket. Előnyük, hogy pontosabbak az eset-kontroll és keresztmetszeti vizsgálatoknál, hártányuk pedig, hogy adott esetben több évig is eltarthatnak.
kontingenciatáblázat
(contingency table)
A kontingenciatáblázat változók gyakorisági eloszlását foglalja össze. Az orvostudományban általában 2 × 2-es táblázat (mátrix), melyben az oszlopok és sorok eltérő tulajdonságokat jelentenek, például egy vizsgálat résztvevőinek nemét, kezelési vagy kontrollcsoportba való tartozást vagy egy adott betegség meglétét.
konfidencia-szint
(confidence level)
A konfidencia-szint (γ) azt fejezi ki, hogy a hipotézisvizsgálat során mennyire vagyunk biztosak a nullhipotézis elvetését/megtartását illető döntésünkben. Szorosan összefügg a szignifikancia-szinttel (α): γ = (1-α). Mivel α értéke az orvostudományokban általában 5%, ezért γ értéke legtöbbször 95%.
korreláció
(correlation)
A korreláció két változó közötti lineáris kapcsolatot jelent. A korreláció irányát a Pearson-féle korrelációs együttható (r) fejezi ki, mely +1 és -1 között vehet fel értéket. A tartományban 3 fontos esetet emelhetünk ki:
- r = 0: A két változó nem korrelál egymással.
- r ≈ +1: A két változó pozitívan korrelál egymással, vagyis az egyiket növelve (csökkentve) a másik is növekszik (csökken).
- r ≈ -1: A két változó negatívan korrelál egymással, vagyis az egyiket növelve (csökkentve) a másik csökken (növekszik).
M
meta-analízis
(meta-analysis)
Statisztikai folyamat a hasonló célkitűzésű orvosi vizsgálatok statisztikai összegzésére és elemzésére. Hasonló a szisztematikus áttekintéshez, de több annál. Például egy adott gyógyszer hatását vizsgáló közlemények résztvevőinek száma így összeadódik, és a bizonyítékok pedig statisztikailag szilárdabb eredményt képezhetnek. A kutatásokat egymáshoz viszonyított pontosságukkal súlyozzák, hogy a megbízhatóbb vizsgálatok eredményei nagyobb arányban legyenek figyelembe véve. Természetesen a különböző vizsgálatok bizonyos mértékben heterogének, azaz több szempontból eltérnek egymástól (tervezettség, résztvevőszám stb.), illetve jelen van a kiküszöbölhetetlen, ún. publikációs torzítás is, mely a pozitív eredmények közzétételének elfogultságát jelenti.
meta-regresszió
(meta-regression)
A meta-regresszió klinikai kutatások meta-analízissel feltárt heterogenitásának további elemzésére szolgáló statisztikai eljárás. A meta-regresszióban a több résztvevőt vizsgáló kutatások nagyobb súlyt kapnak, a hatásmutatót pedig a kezelés hatásnagysága (például átlagok közötti eltérés, esélyhányados vagy relatív kockázat) adja. A vizsgálatok bizonyos jellemzői, az ún. kovariánsok (vagy lehetséges hatásmódosítók) olyan magyarázó változók, melyek kihatással lehetnek a hatásnagyságra. A meta-regresszió a lineáris összefüggéseket vizsgálja a hatásmutató és ezen kovariánsok között.
N
nullhipotézis
(null hypothesis)
A biometriában a nullhipotézis (H0) a hatástalanságot jelenti, ugyanis ekkor feltételezzük azt, hogy a mért adatok változékonysága csak véletlen okokra (biológiai változékonyság, mérési hibák stb.) vezethető vissza. Ideális esetben tehát elvetjük a nullhipotézist, a kezelést pedig hatásosnak tekinthetjük.
normális eloszlás
(normal distribution)
A normális eloszlás (vagy Gauss-eloszlás) a biológiában gyakran előforduló folytonos valószínűségi eloszlás. Sűrűségfüggvényét (függvény, mely megadja egy érték mérésének valószínűségét) jellegzetes alakja miatt haranggörbének is szokták nevezni. A normális eloszlás két jellemző mennyiséggel írható le: az átlagával (μ) és a szórásával (σ). A mérési adatok az átlag körül várhatók a legnagyobb valószínűséggel, az ettől egyre nagyobb eltérés valószínűsége pedig egyre kisebb. Általánosított (standardizált) esetben az átlag nullával (μ = 0), a szórás pedig eggyel egyenlő (σ = 1). Az ilyen eloszlást nevezzük standard normális eloszlásnak (standard normal distribution). Számos emberi mérték normális eloszlást követ, például a testmagasság és az intelligencia-hányados (IQ).
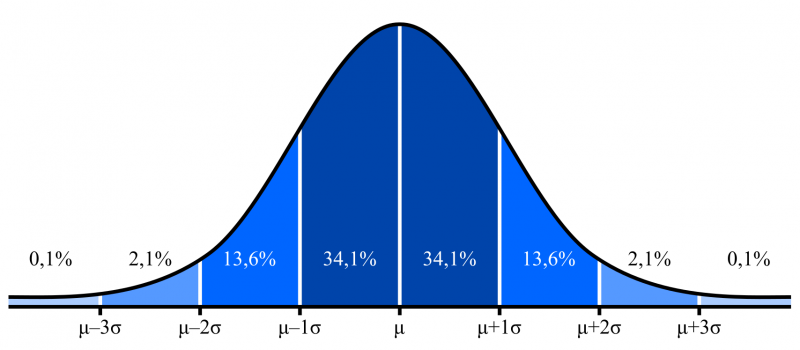
Egy adott x mérési eredmény populációhoz viszonyított helyzetét fejezi ki a z-érték (z-score): z = (x - μ)/σ. Példa: ha a mért testmagasságok átlaga 170 cm, szórása pedig 8 cm, akkor egy 180 cm-es ember a populáció hány százalékánál magasabb? z = (180 cm - 170 cm)/8 cm = 1,25. Ehhez a z-értékhez tartozó arány a táblázat alapján: 0,8944. A mért érték tehát a populáció 89%-ánál magasabb.
O
orvosi tárgyszavak
(Medical Subject Headings, MeSH)
A MeSH egy ingyenesen elérhető orvosi fogalomtár, mely segítségével tárgyszavak alapján lehet orvostudományi közleményeket megkeresni a MEDLINE/PubMed adatbázisban. A tárgyszavak összekapcsolhatók "és"/"vagy" logikai operátorokkal is.
P
p-érték
(p-value)
A p-érték annak valószínűsége, hogy a megfigyelthez hasonlóan szélsőséges hatást mérnénk amellett, hogy a nullhipotézist igaznak feltételezzük. Fontos megjegyezni, hogy a p-érték nem nyújt információt a hatásnagyságról, illetve nem annak valószínűsége, hogy a nullhipotézis igaz vagy az ellenhipotézis hamis.
PICO-modell
(Patients, Intervention, Control, Outcome)
A PICO-modell klinikai vizsgálati kérdések körvonalazásában segít, és a bizonyítékokon alapuló kutatás fontos része.
- Betegek (Patients) = A vizsgálatban résztvevő betegekkel kapcsolatos információk (életkor, nem, kórtörténet, egészségi állapot).
- Beavatkozás (Intervention) = A kutatásban alkalmazott beavatkozás és az ezzel kapcsolatos információk (kezelés hossza, helye, típusa).
- Összehasonlítás (Comparison) = A beavatkozással összehasonlítható másik kezelés, placebo vagy általános ellátás, és az ezzel kapcsolatos információk (kontroll-csoport).
- Kimenetel (Outcome) = A kezelés hatását kifejező mérhető mennyiségek (kórházi felvétel elkerülése, fájdalom, fáradtság, hányinger, fertőzés, halál vagy adott tünet, szindróma vagy betegség megléte).
placebo
A placebo az ún. látszatkezelés, mely során a vizsgált személy a kezelésben használthoz hasonló fizikai tulajdonságú (szín, forma stb.), de hatás nélküli gyógyszert kap (sok esetben cukortaplettákat). Egy klinikai vizsgálatban a placebo-kezelésben részesült csoportban tapasztalható változás a placebo-válaszreakció, ennek eltérése a kezelés nélküli kontrollcsoporttól pedig a placebo-hatás.
PRISMA módszertani ajánlás
(Preferred Reporting Items for Systematic reviews and Meta-Analyses)
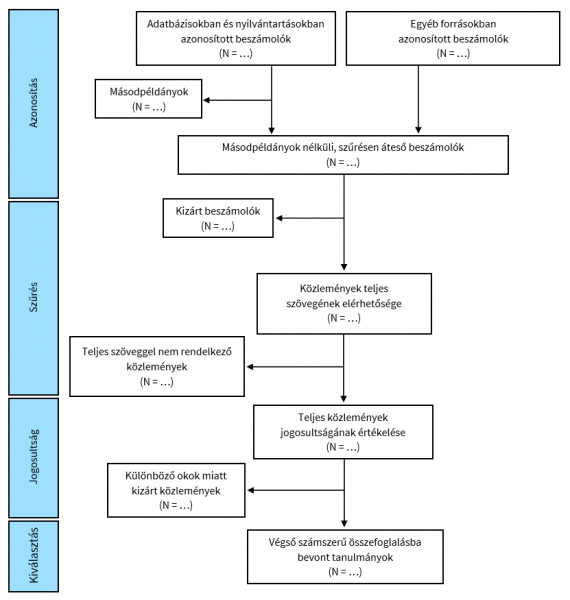
Az információkeresés számszerű nyomon követésére használt eljárás, melyet a randomizált, kontrollált vizsgálatok (RCT-k) esetén alkalmazott CONSORT módszeréhez hasonló folyamatábrával lehet jellemezni. A folyamatábra az alábbi főbb lépéseknél követeli meg az adatforrások számának megadását:
- Azonosítás. Beszámolók keresése adatbázisokban és nyilvántartásokban kulcsszavak alapján, illetve egyéb forrásokban (weboldalak, szervezetek, hivatkozások).
- Másodpéldányok eltávolítása. Bizonyos közlemények párhuzamosan több elektronikus adatbázisba is bekerülnek.
- Cím és absztrakt szerinti szűrés. A kutatás kérdésének megválaszolása szempontjából lényegtelen tanulmányok kizárása.
- Teljes szöveg elérhetősége. Azon tanulmányok kizárása, melyekhez nem található teljes szöveg.
- Jogosultság ellenőrzése. A teljes szövegű, kapcsolódó tanulmányok közül azok kizárása, melyek bizonyos szempontok miatt nem megfelelők (tervezés, kezelés, betegpopuláció).
- A kiválasztott tanulmányok végső száma. Ezek a tanulmányok kerülnek be a végső számszerű összefoglalásba.
protokoll-szerinti elemzés
(per-protocol analysis)
A kezelési csoportok összehasonlítása csak azokkal a résztvevőkkel, akik befejezték a vizsgálatot. A kiértékelés nem veszi figyelembe a vizsgálatból személyes okból kilépő vagy a kezelést mellékhatások miatt abbahagyni kényszerülő résztvevők mérési adatait, hatásmutatóit.
PubMed adatbázis
(PubMed database)
A PubMed egy szabadon hozzáférhető, a MEDLINE elektronikus adatbázisát használó keresőgép, melyben több mint 32 millió orvosbiológiai hivatkozás és absztrakt található. Az adatbázist az egyesült államokbeli Nemzeti Biotechnológiai Információs Központ (NCBI) fejlesztette ki és kezeli 1996 óta.
Q
QUOROM közlemény
(Quality Of Reporting Of Meta-analyses)
A QUOROM közlemény az áttekintések és meta-analízisek folyóiratban való közlése során betartandó irányelveket foglalja össze, és egy 27 elemből álló ellenőrző listát és egy négyrészes folyamatábrát foglal magába. A diagram célja, hogy átláthatóvá tegye a kutatók által a tanulmányok bevonása vagy kizárás kapcsán hozott döntéseit, csökkentve ezzel a hatás meghatározása során fellépő torzításokat. A QUOROM közleményt 2009-ben frissítették a szisztematikus áttekintések tudományában bekövetkezett számos előrelépés figyelembevételével, az új ajánlásnak pedig a PRISMA nevet adták.
R
randomizált, kontrollált vizsgálat
(Randomized Controlled Trial, RCT)
A randomizált, kontrollált vizsgálatokban a résztvevőket véletlenszerűen sorolják be a vizsgálatban meghatározott kettő vagy több csoport egyikébe, ezt nevezzük randomizációnak. A kontrollcsoport (kontrolláltság) tagjai nem esnek át kezelésen (intervención), a másik vagy többi csoport tagjai azonban valamilyen kezelésben részesülnek. A kezelés hatékonyságát a kezelt és a kontrollcsoport tagjainál mért egészségügyi kimenetelek közti különbség jelenti. Az RCT-k prospektív vizsgálatok, mivel megtervezésük megelőzi magát a vizsgálatot.
Fontos szempont a kezelés titkosítása, hiszen például a placebo-hatás vizsgálata csak úgy oldható meg, ha a résztvevő nem tudja, hogy valódi vagy placebo kezelést kapott-e. A vizsgálati elrendezést, vagyis azt, hogy a résztvevők melyik csoportba tartoznak csak a kezelés lezárulása után közlik:
- egyszeres vak (single-blind) vizsgálat esetén csak a résztvevők nem,
- kettős vak (double-blind) vizsgálat esetén a résztvevők és a vizsgálatot végzők sem,
- háromszoros vak (triple-blind) vizsgálat esetén a résztvevők, a vizsgálatot végzők és az adatokat elemzők sem
tudják ezt.
regresszió-analízis
(regression analysis)
A regresszió-analízis egy függő változó és egy vagy több független változó közötti kapcsolat erősségének meghatározására szolgáló statisztikai módszer. Az összefüggés legegyszerűbb formája a lineáris regresszió, vagyis amikor a függő (y) változót a független (x) változó függvényében ábrázolva a pontok egy egyenessel közelíthetők. Az egyenes egyenlete y(x) = ax + b, ahol az a és b paraméterek valós számok.
relatív gyakoriság
(relative frequency)
Egy kimenetel bekövetkezésének száma osztva az összes próba számával egy kísérletsorozatban. Nagyszámú kísérlet esetén a kimenetel valószínűségéhez közelítő érték. Példa: egy 100 próbából álló kísérletsorozatban egy szabályos dobókockával 21 alkalommal dobunk hatos értéket. A relatív gyakoriság ekkor: 21/100 = 0,21 = 21%. A próbák számának növelésével a relatív gyakoriság egyre közelebb kerül a kimenetel valószínűségéhez (~16,7%).
relatív kockázat
(Relative Risk vagy Risk Ratio, RR)
A relatív kockázat egy esemény bekövetkezésének valószínűség-aránya egy kezelési és egy másik, eltérő tulajdonságú (életvitel, fizikai állapot, étrend, szociális helyzet stb.) kontrollcsoportban. Tekintsük az alábbi kontingenciatáblázatot:

A relatív kockázat (RR) a táblázat jelölései alapján:
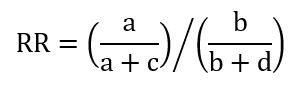
Értéke az alábbi három tartomány egyikébe esik:
- RR < 1: a kezelés lecsökkentette az esemény bekövetkezésének kockázatát, vagyis védő tényezőnek tekinthető.
- RR = 1: a kezelés nem változtatta meg az esemény bekövetkezésének kockázatát.
- RR > 1: a kezelés megnövelte az esemény bekövetkezésének kockázatát, vagyis kockázati tényezőnek tekinthető.
Példa: Ha egy 10.000 fős kezelési csoportban egy betegség 560 főnél, illetve egy ugyanekkora kontrollcsoportban 660 főnél jelentkezik, akkor a relatív kockázat: (560/10.000) / (660/10.000) = 0,056/0,066 = 0,85. A kezelés tehát védő tényezőnek minősül a betegség tekintetében.
Fontos megjegyezni, hogy a relatív kockázat önmagában nem tartalmaz elegendő információt a populációról, hiszen arányszámot fejez ki.
relatív kockázat-csökkentés és -növelés
(Relative Risk Reduction, RRR / Relative Risk Increase, RRI)
A relatív kockázat-csökkentés (vagy hatékonyság) a kezelési csoport kockázatának relatív csökkenése egy kontrollcsoporthoz képest. Ha egy kezelés (intervenció) csökkenti egy káros egészségügyi kimenetel kockázatát (pozitív hatás), akkor a relatív kockázat-csökkentés (RRR) a táblázat jelölései alapján:
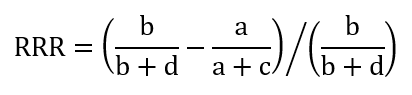
Példa: Ha egy 10.000 fős kezelési csoportban egy betegség 560 főnél, illetve egy ugyanekkora kontrollcsoportban 660 főnél jelentkezik, akkor a relatív kockázat: [(660/10.000)-(560/10.000)] / (660/10.000) = (0,066-0,056)/0,066 = 0,15. A kezelés tehát 15%-kal csökkentette a betegség relatív kockázatát.
Ha egy kezelés növeli egy káros egészségügyi kimenetel kockázatát (negatív hatás), akkor a relatív kockázat-növelés (RRI) a táblázat jelölései alapján:
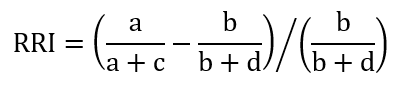
S
Scopus adatbázis
(Scopus database)
A Scopus a lektorált szakirodalom legnagyobb absztrakt és idézet adatbázisa, mely 2004 óta segíti a kutatókat a megbízható adatok és az analitikai eszközök beazonosításában. Több mint 40.000 ellenőrzött könyvsorozatot, szaklapot és tudományos folyóiratot jegyez, közel 12.000 kiadótól.
Sz
szignifikancia-szint
(significance level)
A szignifikancia-szint (α) a hipotézisvizsgálat során használt statisztikai küszöbérték. Azt fejezi ki, hogy a mért adatok alapján milyen valószínűséggel vetnénk el a nullhipotézist, ha azt kezdetben igaznak feltételezzük. Szorosan összefügg a konfidencia-szinttel (γ): α = (1-γ). A szignifikancia-szint értéke az orvostudományban általában 5%.
szisztematikus áttekintés
(systematic review)
A szisztematikus áttekintés egy folyamat, ami az alábbi lépésekből áll:
- a kutatási kérdés megfogalmazása, vagyis az áttekintés témája
- a kiválasztási és kizárási kritériumok meghatározása
- adatbázisban történő szakirodalomkeresés
- a szakirodalmak kritikus kiválasztása, minőségi értékelése
- a kiválasztott szakirodalmak adatainak feldolgozása, összefoglalása
A szisztematikus áttekintések inkább csak különálló vizsgálatok összefoglalásai, és a meta-analízisekkel ellentétben nem tesztelnek hipotéziseket.
T
t-eloszlás
(t-distribution)
A t-eloszlás szimmetrikus valószínűségi eloszlás, melynek görbe-meredeksége kis elemszámok esetén nagyobb, mint a normális eloszlásé, nagy elemszámok esetén (n>30) viszont már szinte megegyezik a normális eloszlással. A hipotézisvizsgálat során meghatározandó kritikus t-érték a megfelelő elemszám által megadott t-eloszlásból származik, egy kiválasztott szignifikancia-szint (α, általában 0,05) mellett.
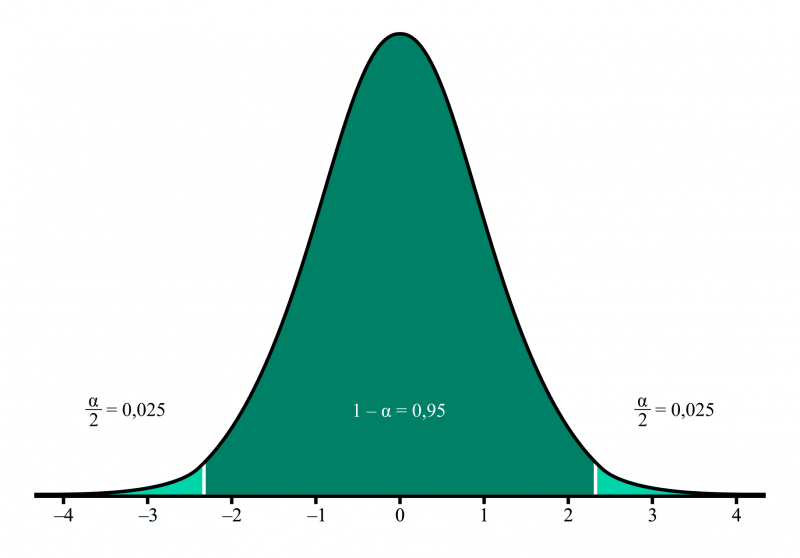
t-próba
(Student's t-test)
Statisztikai eljárás, mellyel eldönthetjük, hogy egy adatsor és egy érték (egymintás t-próba) vagy két adatsor (kétmintás t-próba) közötti eltérés szignifikánsnak tekinthető-e. A módszert hipotézisvizsgálat során alkalmazzuk, például egy randomizált, kontrollált vizsgálatban. A nullhipotézis szerint a kezelt és a kontrollcsoportba sorolt emberek mérési adatainak eloszlása statisztikailag megegyezik egymással, vagyis nincs szignifikáns különbség köztük - a kezelés hatástalan. Egy szignifikancia-szint (α) megválasztása után számítsuk ki a próbastatisztikát, majd hasonlítsuk össze a t-táblázatban található, megfelelő paraméterekkel rendelkező kritikus t-értékkel. Ha a számított t-érték nagyobb, mint a kritikus, akkor nem vethetjük el a nullhipotézist, ellenkező esetben viszont megtehetjük ezt.
V
valószínűség
(probability)
Elméleti érték, egy kimenetel bekövetkezésének száma osztva a lehetséges kimenetelek számával. Egy kísérletsorozatban mért relatív gyakoriság nagy próbaszám mellett ehhez az értékhez közelít. Példa: egy szabályos dobókockával hatos érték dobásának valószínűsége: 1/6 ≈ 0,167 ≈ 16,7%.
véletlenszerű besorolás / randomizálás
(randomization)
A véletlenszerű besorolás a torzítás-csökkentés fontos részét képzi a klinikai kutatásokban. Ezzel érhető el, hogy a résztvevők ugyanolyan valószínűséggel kerülhetnek be a kettő vagy több vizsgálati csoportba, ahol így az alanyok különböző tulajdonságai egyformán lesznek reprezentálva, és ahol az egyetlen szignifikáns különbséget a beavatkozás fajtája fogja jelenteni.
A fenti fogalomtár részben Decsi Tamás - A bizonyítékokon alapuló orvoslás c. könyve alapján készült.
Német nyelvű Cochrane-fogalomtár

